La pastilla está autorizada para tratar el contagio leve por Covid en personas desde los 12 años de edad y se debe tomar a los cinco días posteriores de presentar los primeros síntomas. Más detalles, a continuación.
A dos años del inicio de la pandemia, y con más de 500 millones de infectados a nivel global, los países avanzan a ritmo sostenido con sus campañas de vacunación, mientras que los casos de coronavirus bajan lentamente tras el impacto de la variante Ómicron en diciembre y enero.
Según los datos relevados por el sitio OurWorldInData, el 65% de la población mundial ha recibido al menos una dosis del suero contra el coronavirus, y a nivel global se llevan administradas 11.480 millones de dosis. Se estima que diariamente se colocan 10,7 millones de sueros aunque en los países de bajos ingresos apenas el 15,2% de las personas han recibido una dosis.
En este contexto, cabe destacar, se buscan distintas formas de subir las defensas de la población para así combatir al virus. La OMS, por su parte, suele actualizar regularmente sus recomendaciones de tratamientos contra el covid, apoyándose en ensayos clínicos realizados con diferentes tipos de pacientes.
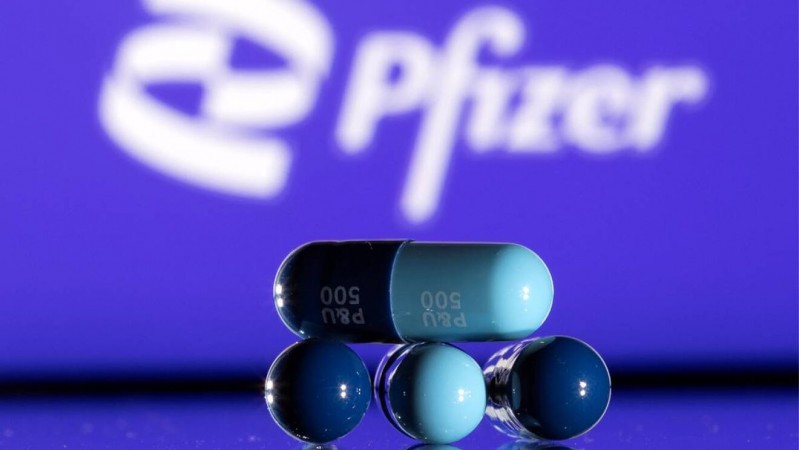
A los anteriores medicamentos se suman las pastillas de algunas farmacéuticas, como Pfizer y Merck, que ya han sido autorizadas por la OMS y el personal sanitario. A este aval se sumó también la Agencia Europea del Medicamento (EMA) que, a finales de 2021, recomendó a los países del bloque comunitario usar el tratamiento oral de Pfizer.
Este nuevo medicamento se denomina: Paxlovid. Está autorizada también por la Administración de Alimentos y Fármacos de Estados Unidos (FDA) y, de acuerdo con un comunicado de la misma agencia, "aprobada para lidiar con el contagio leve de covid-19 en personas desde los 12 años de edad"
Fuente El Cronista









Dejanos tu comentario
Su comentario estará disponible a la brevedad.